注意:此页面搜索的是所有试题
佳木斯大学语言治疗学
体系由初态A经不同的不可逆途径达到终态B时,其熵变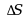 应如何( )
应如何( )
· 各不相同
· 都相同
· 不等于经可逆途径的熵变
· 不一定相同
影响理想气体化学反应标准平衡常数K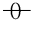 的因素有( )。
的因素有( )。
·压力
·温度
·催化剂
· 浓度
下述说法中哪一个正确:( )
· 热是体系中微观粒子平均平动能的量度;
· 温度是体系所储存能量的量度
· 温度是体系中微观粒子平均能量的量度;
· 温度是体系中微观粒子平均平动能的量度
在一个绝热的真空容器中,灌满 373 K 和压力为 101.325 kPa的纯水,不留一点空隙,这时水的饱和蒸汽压 ( )
· 等于零
· 大于 101.325 kPa
· 小于 101.325 kPa
·等于 101.325 kPa
实际气体的压力(p)和体积(V)与理想相比,分别会发生的偏差为 ( )
· p, V 都发生正偏差
· p,V 都发生负偏差
· p 正偏差, V 负偏差
· p 负偏差, V 正偏差
在273.15K,2pθ时,水的化学势与冰的化学势之间的关系如何:( )
· 前者高
· 前者低
· 相等
· 不可比较
关于偏摩尔量,下列叙述中不正确的是:( )
· 偏摩尔量是状态函数,其值与物质的数量无关;
· 在多组分多相体系中不存在偏摩尔量
· 体系的强度性质没有偏摩尔量;
· 偏摩尔量的值只能大于或等于零
下面的说法符合热力学第一定律的是( )
· 在一完全绝热且边界为刚性的密闭容器中发生化学反应时, 其内能一定变化
· 在无功过程中, 内能变化等于过程热, 这表明内能增量不一定与热力学过程无关。
· 封闭系统在指定的两个平衡态之间经历绝热变化时, 系统所做的功与途径无关。
· 气体在绝热膨胀或绝热压缩过程中, 其内能的变化值与过程完成的方式无关。
如图,将CuSO4水溶液置于绝热箱中,插入两个铜电极,以蓄电池为电源进行电解,可以看作封闭体系的是( )。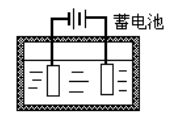
·绝热箱中所有物质
· 两个铜电极
· 蓄电池和铜电极
· CuSO4水溶液
热力学第一定律ΔU=Q+W 只适用于 ( )
·单纯状态变化
·相变化
·化学变化
·封闭物系的任何变化
与物质的生成热有关的下列表述中不正确的是 ( )
·标准状态下单质的生成热都规定为零
·化合物的生成热一定不为零
·很多物质的生成热都不能用实验直接测量
·通常所使用的物质的标准生成热数据实际上都是相对值
下列过程中, 系统内能变化不为零的是 ( )
·不可逆循环过程
·可逆循环过程
·两种理想气体的混合过程
·纯液体的真空蒸发过程
盖斯定律包含了两个重要问题, 即 ( )
·热力学第一定律和热力学第三定律
·热力学第一定律及热的基本性质
·热力学第三定律及热的基本性质
·热力学第一定律及状态函数的基本特征
ΔG=0 的过程应满足的条件是 ( )
·等温等压且非体积功为零的可逆过程
·等温等压且非体积功为零的过程
·等温等容且非体积功为零的过程
·可逆绝热过程
对任一过程,与反应途径无关的是 ( )
·体系的内能变化
·体系对外作的功
·体系得到的功
·体系吸收的热
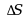 应如何( )
应如何( )· 各不相同
· 都相同
· 不等于经可逆途径的熵变
· 不一定相同
影响理想气体化学反应标准平衡常数K
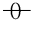 的因素有( )。
的因素有( )。·压力
·温度
·催化剂
· 浓度
下述说法中哪一个正确:( )
· 热是体系中微观粒子平均平动能的量度;
· 温度是体系所储存能量的量度
· 温度是体系中微观粒子平均能量的量度;
· 温度是体系中微观粒子平均平动能的量度
在一个绝热的真空容器中,灌满 373 K 和压力为 101.325 kPa的纯水,不留一点空隙,这时水的饱和蒸汽压 ( )
· 等于零
· 大于 101.325 kPa
· 小于 101.325 kPa
·等于 101.325 kPa
实际气体的压力(p)和体积(V)与理想相比,分别会发生的偏差为 ( )
· p, V 都发生正偏差
· p,V 都发生负偏差
· p 正偏差, V 负偏差
· p 负偏差, V 正偏差
在273.15K,2pθ时,水的化学势与冰的化学势之间的关系如何:( )
· 前者高
· 前者低
· 相等
· 不可比较
关于偏摩尔量,下列叙述中不正确的是:( )
· 偏摩尔量是状态函数,其值与物质的数量无关;
· 在多组分多相体系中不存在偏摩尔量
· 体系的强度性质没有偏摩尔量;
· 偏摩尔量的值只能大于或等于零
下面的说法符合热力学第一定律的是( )
· 在一完全绝热且边界为刚性的密闭容器中发生化学反应时, 其内能一定变化
· 在无功过程中, 内能变化等于过程热, 这表明内能增量不一定与热力学过程无关。
· 封闭系统在指定的两个平衡态之间经历绝热变化时, 系统所做的功与途径无关。
· 气体在绝热膨胀或绝热压缩过程中, 其内能的变化值与过程完成的方式无关。
如图,将CuSO4水溶液置于绝热箱中,插入两个铜电极,以蓄电池为电源进行电解,可以看作封闭体系的是( )。

·绝热箱中所有物质
· 两个铜电极
· 蓄电池和铜电极
· CuSO4水溶液
热力学第一定律ΔU=Q+W 只适用于 ( )
·单纯状态变化
·相变化
·化学变化
·封闭物系的任何变化
与物质的生成热有关的下列表述中不正确的是 ( )
·标准状态下单质的生成热都规定为零
·化合物的生成热一定不为零
·很多物质的生成热都不能用实验直接测量
·通常所使用的物质的标准生成热数据实际上都是相对值
下列过程中, 系统内能变化不为零的是 ( )
·不可逆循环过程
·可逆循环过程
·两种理想气体的混合过程
·纯液体的真空蒸发过程
盖斯定律包含了两个重要问题, 即 ( )
·热力学第一定律和热力学第三定律
·热力学第一定律及热的基本性质
·热力学第三定律及热的基本性质
·热力学第一定律及状态函数的基本特征
ΔG=0 的过程应满足的条件是 ( )
·等温等压且非体积功为零的可逆过程
·等温等压且非体积功为零的过程
·等温等容且非体积功为零的过程
·可逆绝热过程
对任一过程,与反应途径无关的是 ( )
·体系的内能变化
·体系对外作的功
·体系得到的功
·体系吸收的热